
近二十年来,我国超重/肥胖的患病率逐年增长,呈流行态势。根据国家体育总局、教育部2015年11月底发布的《2014年国民体质监测公报》,虽然我国国民体质总体水平有所增长,但无论是青少年学生人群还是成年人、老年人人群中,超重、肥胖现象仍然呈持续增长的势头。若以BMI值“24”为超重的界限,BMI值“28”为肥胖的界限,2014年与2010年两次国民体质监测中各人群的超重率与肥胖率如图1、图2所示。
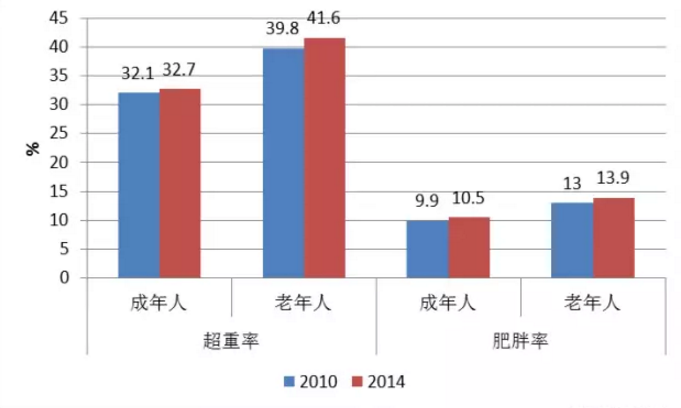
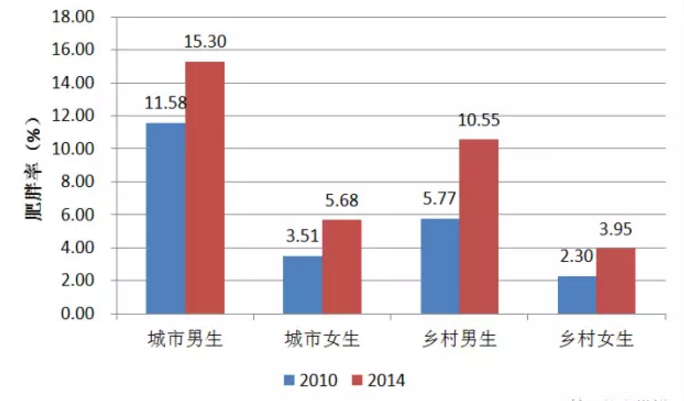
除了体型与外貌的不足,超重/肥胖症患者诸多疾病的发病风险也有所上升(表1)。
表1 肥胖者发生肥胖相关疾病或症状的相对危险度*
(摘自《中国成人超重与肥胖症预防控制指南(试行)》以及国际癌症研究机构(IARC)于2016年8月发表的Body Fatnessand Cancer-Viewpoint of the IARC Group一文)

二、肥胖的药物治
大多数肥胖症患者在认识到肥胖对健康的危害后,在医疗保健人员的指导下控制饮食量、养活脂肪摄入,并增加体育活动,常可使体重显着减轻。但由于各种原因体重仍然不能减低者,或行为疗法欠佳者,可考虑用药物辅助减重。如果有的肥胖症患者因担心增加体力活动可加重原有疾病或使病情出现新的变化,也有必要采用药物辅助减重。下文即对国内外批准的减肥药物进行了评价。
(一)各国批准情况
目前国内外可用于长期体重控制的药物如表2所示。
表2 用于长期体重控制的药物
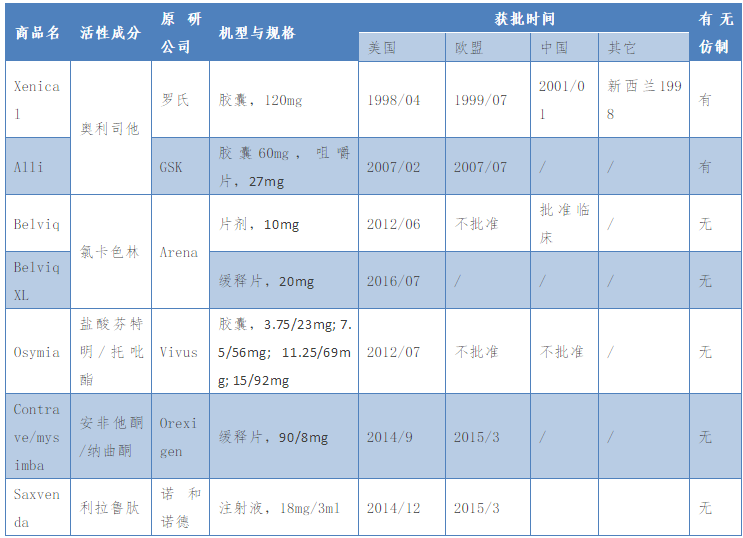
此外,FDA还于2015年4月29日批准了脱氧胆酸(Deoxycholic acid)注射液用于治疗双下巴,规格为20mg/2mL,商品名为Kybella;FDA还批准了盐酸芬特明(Phentermine Hydrochloride)的多种制剂,但此两种药物均不用于体重的长期控制;日本厚生劳动省于2013年9月批准了奥利司他的同作用机制药物Cetilistat,但该药至今未上市。
(二)作用机制
常用的减肥药的作用机制如表3与图3所示。
表3 常用减肥药的作用机制
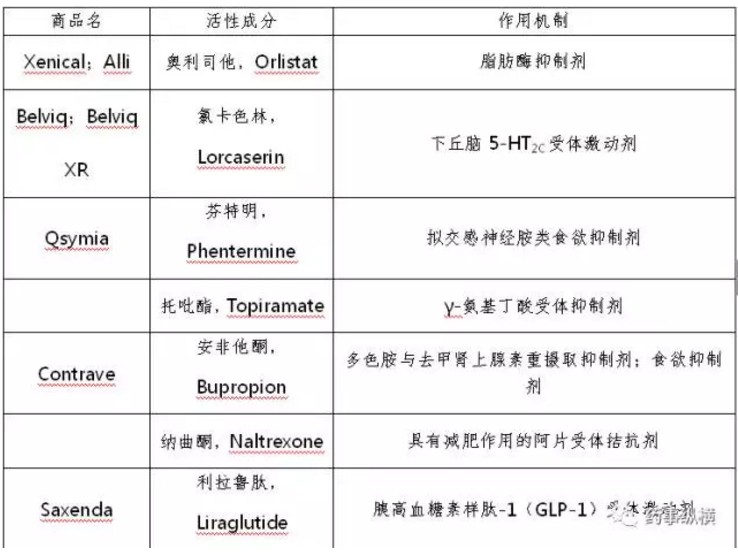
表3中长期体重控制用药物的作用机制如下图所示。
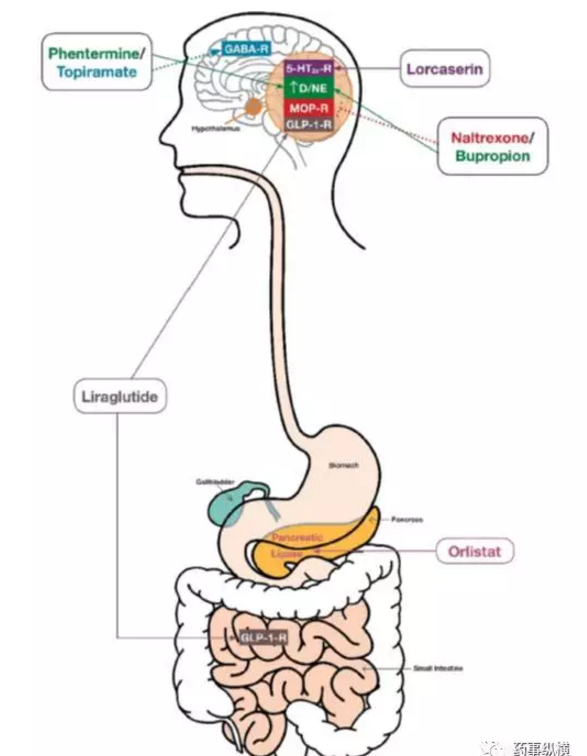
图3-获FDA批准的长期减肥用处方药的作用机制概述。点状箭头所示即为可能的机制。5-HT2C-R= 5-羟色胺2C受体;D/NE=多巴胺/去甲肾上腺素;GABA-R = γ-氨基丁酸受体;GLP-1-R =胰高血糖素样肽-1受体;MOP-R = μ-阿片受体。
(三)临床评价
试验概况
验证各种减肥药有效性与安全性的临床试验设计如表4所示。
表4 减肥药的临床试验设计
药物 试验 人群基础特征 干预方法 时长 Xenical XENDOS 萄糖耐受正常(79%)与受损(21%)的超重与肥胖患者(BMI≥27kg/m2) 奥利司他,p.o.,120mg,TID; 安慰剂 4年 Xenical 中国验证试验 BMI在25~40kg/m2之间的中国超重与肥胖患者 奥利司他,p.o.,120mg,TID; 安慰剂 半年 Belviq BLOOM 第1年:BMI在27~45kg/m2之间的超重与肥胖患者;第2年:第1年氯卡色林组内患者 氯卡色林,p.o.,10mg,QD; 安慰剂 2年 BLOSSOM BMI在30~45 kg/m2之间的患者或BMI在27~29.9kg/m2之间且同时存在至少1种并发症的患者 氯卡色林,p.o.,10mg,QD; 氯卡色林,p.o.,10mg,BID 安慰剂 1年 BLOOM-DM BMI在27~45kg/m2之间且并发有Ⅱ型糖尿病的患者 氯卡色林,p.o.,10mg,QD; 氯卡色林,p.o.,10mg,BID 安慰剂 1年 Qsymia CONQUER BMI在27~45kg/m2之间且至少并发有两种并发症的患者 托吡酯/芬特明,p.o.,7.5/46mg,QD; 托吡酯/芬特明,p.o.,15/92mg,QD; 安慰剂 1年 EQUIP BMI≥35kg/m2的重度肥胖患者 托吡酯/芬特明,p.o.,3.75/23mg,QD; 托吡酯/芬特明,p.o.,15/92mg,QD; 安慰剂 1年 SEQUEL (CONQUER的延期试验) BMI在27~45kg/m2之间且至少并发有两种并发症的患者 托吡酯/芬特明,p.o.,7.5/46mg,QD; 托吡酯/芬特明,p.o.,15/92mg,QD; 安慰剂 1年 Contrave COR-Ⅰ BMI在30~45kg/m2之间的患者或BMI在27~45kg/m2之间且并发有血脂异常或受控的高血压的患者 安非他酮/纳曲酮,p.o.,每日剂量360/16mg; 安非他酮/纳曲酮,p.o.,每日剂量360/32mg; 安慰剂 56周 COR-Ⅱ BMI在30~45kg/m2之间的患者或BMI在27~45kg/m2之间且并发有血脂异常或受控的高血压的患者 安非他酮/纳曲酮,p.o.,每日剂量360/32mg; 安慰剂 56周 COR-BMOD BMI在30~45kg/m2之间的患者或BMI在27~45kg/m2之间且并发有血脂异常或受控的高血压的患者 安非他酮/纳曲酮,p.o.,每日剂量360/32mg; 安慰剂 两组均接受强化的行为干预 56周 COR-Diabetes BMI在27~45kg/m2之间且并发有Ⅱ型糖尿病的患者 安非他酮/纳曲酮,p.o.,每日剂量360/32mg; 安慰剂 56周 Saxenda SCALE Maintenance BMI≥30kg/m2的患者或BMI≥27kg/m2且带有并发症的患者 利拉鲁肽,i.c.,3mg,QD; 安慰剂 1年 SCALE Diabetes BMI≥27kg/m2且并发有Ⅱ型糖尿病的患者 利拉鲁肽,i.c.,3mg,QD; 安慰剂 1年 SCALE Obesity and Prediabetes 糖尿病前期患者,包括BMI≥30kg/m2的患者或BMI≥27kg/m2的患者且并发的血脂异常或高血压未接受治疗的患者 利拉鲁肽,i.c.,3mg,QD; 安慰剂 1年
2. 有效性特征
(1)对体重的影响
常用减肥药物在临床试验中对体重影响分别如表5所示。
此外,一项安慰剂对照临床试验的meta分析结果显示,奥利司他(120mg,一天三次)施用于未并发有Ⅱ型糖尿病的超重与肥胖症患者中后,患者体重比安慰剂用药多降低2.9kg或2.9%。该项分析中,奥利司他组实现≥5%与≥10%减肥效果的患者所占比例分别比安慰剂组高21%与10%。在并发有超重与肥胖症的Ⅱ型糖尿病患者中,奥利司他用药后所导致的体重减轻程度比安慰剂高2.3kg或2.6%。
(2)对心脏代谢参数的影响(表6)
表6 减肥药物对心脏代谢参数的影响
商品名 | 临床试验 | 报告的 时长 (年) | 偏离基线的平均变化幅度(药物 vs 安慰剂) | ||||
SBP (mmHg) | DBP (mmHg) | LDL-C(%) | HDL-C(%) | 心率(次/分钟) | |||
Xenical | XENDOS | 4 | -4.9 vs -3.4a | -2.6 vs -1.9 a | -12.8 vs -5.1a | 6.5vs 9.1 a | NA |
Belviq | BLOOM | 1 | -1.4 vs -0.8a | -1.1 vs -0.6 a | 2.9 vs 4.0 a | 0.1 vs -0.2 | -2.0 vs -1.6 a |
BLOSSOM | 1 | -1.9 vs -1.2 | -1.9 vs -1.4 | 0.3 vs 1.7 | 3.7 vs 1.3 | -2.3 vs -1.6 | |
BLOOM-DM | 1 | -0.8 vs -0.9 | 1.1 vs -0.7 | 4.2 vs 5.0 | 5.2 vs 1.6 a | -2.0 vs -0.4 a | |
Qsymia | CONQUERb | 1 | -5.6 vs -2.4a | -3.8 vs -2.7 | -6.9 vs -4.1a | 6.8 vs 1.2 a | 1.7 vs -0.1 a |
EQUIPb | 1 | -2.9 vs 0.9 a,c | -1.5 vs 0.4 a,c | -8.4 vs -5.5a | 3.5 vs 0.0 a | 1.2 vs -0.2 | |
SEQUELb | 2 | -4.3 vs -3.2 | -3.5 vs -3.9 | -5.6 vs -10.7a | 11.9 vs 4.7 a | 1.7 vs 0.4 | |
Contrave | COR-Ⅰ | 1 | -0.1 vs -1.9a | 0.0 vs -0.9a | -0.1 vs -0.1d | 0.1 vs 0.0a,d | 1.0 vs -0.1a |
COR-Ⅱ | 1 | 0.6 vs -0.5 a | 0.4 vs 0.3 | -6.2 vs -2.1a,e | 3.6 vs -0.9a,e | 0.8 vs -0.3a | |
COR-BMOD | 1 | -1.3 vs -3.9a | -1.4 vs -2.8 a | 7.1 vs 10.0 | 9.4 vs 2.8 a | 1.1 vs 0.2 | |
COR-Diabetes | 1 | 0.0 vs -1.1 | -1.1 vs -1.5 | -1.4 vs 0.0e | 3.0 vs -0.3 a,e | NA | |
Saxenda | SCALE Maintenance | 1 | 0.2 vs 2.8 a | 1.4 vs 1.2 | 0.2 vs 0.3d | 0.2 vs 0.1d | 3.6 vs 2.4 |
SCALE Diabetesf | |||||||
SCALE Obesity and Prediabetes | 1 | -4.2 vs -1.5 a | -2.6 vs -1.9 a | -3.0 vs -1.0 a | 2.3 vs 0.7 a | 2.5 vs 0.1 a | |
注:若无特殊说明,所有数值均为临床剂量的数值。 a 药物与安慰剂之间有显着差异 b 此处报告的数值为高剂量芬特明/托吡酯(15mg/92mg)与安慰剂的数值 c报告值为与基线相比的百分变化率 d 报告值为与基线相比的绝对变化值(mmol/L) e 报告值为与基线相比的绝对变化值(mg/dL) f 尚未发现试验数据 | |||||||
3. 安全性特征(表7)
(四)市场与专利
2016年刊登于Lancet杂志的 Management of Obesity一文对各种减肥药的优势与劣势进行了比较,如表8所示。
表8 常用减肥药的优劣分析
奥利司他,商品名Xenical,Alli-老牌减肥药,安全,全球普遍使用
奥利司他是全球唯一的OTC减肥药,本品因为无全身吸收、对中枢神经系统、心血管系统无作用等诸多特点,而被刊登于Lancet的Management of Obesity一文评价为“是最安全的减肥药之一”。奥利司他胶囊(Xenical与Alli)曾经给罗氏公司与葛兰素史克带来巨大的商业回报。2013年7月15日刊登在《21世纪经济报导》的《奥利司他:最后的OTC减肥药》援自变量据称,Xenical上市后就销量惊人,第二年销售额已达6亿美元,2007年这一产品的销售额被指逼近20亿美元;2011年葛兰素史克Alli的全球销售额亦达9300万元。此外,FDA于2010年5月发布的通告指出,全球范围内约有4000万人使用了Xenical或Alli;2012年2月EMA的审查报告则指出,1997年至2011年1月间,全球共有超过5300万人使用了Xenical或Alli,其中欧盟地区就有2000多万人。
虽然截止2007年,Xenical的全球累计销售额已超过50亿美元,但自2008年开始,Xenical的销售迅速进入萎缩时期,2009与2010年,全球销售额分别同比降低21%与15%,其中2010年3.37亿元的销售额水平,还不到2002年上市初期7.63亿元的一半。
对于Xenical销售额迅速萎缩的原因,可能是由于专利到期后的仿制药上市所造成的冲击,从而导致罗氏公司调整了产品重点。奥利司他化合物专利US4598089优先权日期为1983年6月22日,2003~2004年起,全球各国同族专利先后到期。美国专利虽然被获准延期,也于2009年6月18日到期。奥利司他的药用晶型(B型)最早公开于期刊文献中,无专利保护。虽然橙皮书与Dailymed的数据库均指出US6004996是奥利司他的组合物专利,但该专利的各国同族专利已被多家公司成功规避,从而导致大量奥利司他仿制药涌入市场。根据NEWPORT数据库下的DOSAGEFORM子数据库,奥利司他制剂已在全球70多个国家上市,涉及200多家生产企业。
而就国内市场而言,2009年与2010年,芬氟拉明与西布曲明(曲美的活性成分)先后因为不良反应被撤出中国市场,这就使奥利司他成为国内仅存的化学减肥药,也是唯一的OTC减肥药。而罗氏公司于2010年停止了赛尼可在中国的销售,从而为奥利司他国内厂家创造了巨大的发展空间。目前,持有奥利司他制剂批文的国内厂家如表9所示。
2015年4月,碧生源宣布与浙江海正药业股份有限公司合作开展奥利司他产品的销售(商标名:来利),使其营销版图从减肥保健茶市场延伸至减肥药品市场。根据该公司的年报,2015年来利品牌销售额为6340万元人民币。2016年中期报告未披露本来利的具体销售额,但声称其持续增长。
2. 芬特明/托吡酯复方,商品名Qysmia-闭门造车,回天乏力
从数据可以看出,芬特明/托吡酯是减肥效果最明显的药物,而且Thomson Reuters报告也认为该药的减肥效果优于氯卡色林或奥利司他,并且优于盐酸芬特明与托吡酯联合用药的效果。此外,有试验表明,该药还可以改善包括血压、血脂与血糖在内的诸多心血管与代谢风险因子。基于其优异的有效性,该药上市前后,曾被普遍看好。但上市后的销售业绩却表现平平,根据Vivus公司的年报,2013、2014与2015年Qsymia的销售额分别仅为4198万、7663万与8418万美元,远低于预期。
对于出现上述情况困局的原因,除了Qsymia自身安全性所引起的担忧,与用药需要剂量滴定而给患者造成的不便,分析人士普遍认为,昂贵的成本与未被纳入医疗保险体系,使患者对Qsymia望而却步。此外,Qsymia还面临来自于价格低廉的老牌减肥药奥利司他以及后来上市的氯卡色林等品种的激烈竞争。而且芬特明属于Ⅳ类管制品,这限制了Qsymia的销售渠道。虽然Vivus公司启动了相关的患者支持计划,甚至不惜降低价格来吸收患者坚持长期用药,但是2016年前3季度Qsymia的处方数量仅为34.2万,同比下降了21.2%。
除了美国国内市场表示差强人意以外,Qsymia在美国以外国家与地区的行政审批形势也不容乐观。EMA的CHMP在FDA批准Qsymia后的2012年12月出于安全性的考虑,而推荐不批准本品(商品名为Qsiva),EMA则在2013年2月正式拒绝了Qsiva的上市申请,此后Vivus公司未采取进一步的措施。根据Vivus公司的Press Release与SEC报表,Qsymia未在美国以外的其他地区上市,而且Vivus公司也未与其他公司签定Qsymia的经销协议。
就中国的申报而言,Vivus公司的中国CRO合作方杭州泰格医药科技股份有限公司所递交的盐酸芬特明托吡酯胶囊进口临床试验申报两次被中国CDE拒绝批准,而国内的申报公司也均未被批准临床。业内人士表示,导致盐酸芬特明托吡酯胶囊注册申报全军覆没的原因是国内没有盐酸芬特明单方的上市品种。
Qsymia在中国的核心专利如表10所示。
表10 Qsymia在中国的核心专利
3. 氯卡色林,商品名Belvqi-忍痛割爱,还是借力用力
Belvqi与Qsymia同一年在美国上市,而其市场表现似乎与Qsymia同命相怜,同样因为诸多因素而市场表现平平。而且2013年5月,Arena公司撤回了氯卡色林在欧洲的上市申请(MAA),这给氯卡色林的市场前景蒙上了阴影。根据该公司财务数据,2016年第3季度Arena公司的总收入为1920万美元,其中,Belviq销售额330万美元,卫材公司的里程碑付款1100万美元。
2017年1月4日,Arena与卫材公司修改了双方先前签订的Belvqi经销与供货协议,将全球的经销权都转给了卫材公司。消息发布的当天,Belviq的股价上升了7.33%。但有文章将Arena公司此举描述为“Dump”,究竟是忍痛割爱还是借力用力,就决定于卫材公司全球范围内的销售团队能否使氯卡色林的销售额是否会有所起色。
当然,2016下半年,Belviq也有诸多令人喜悦的好消息,比如缓释制剂的上市,墨西哥、巴西等国相继批准氯卡色林上市销售。
就国内而言,根据药智网信息,卫材公司申报的盐酸氯卡色林片已获批临床,而国内企业中除了济南百诺医药科技开发有限公司申报的盐酸氯卡色林片未获准临床,其他均已批准临床。
Belviq在中国的核心专利如表11所示。
表11 Belviq在中国的核心专利
4. 安非他酮/纳曲酮复方,商品名Contrave(美国),Mysimba(欧洲)-后起之秀,全球发力
Contrave原先由Orexigen公司生产,武田制药负责销售。但2016年3月,两家公司中止了Contrave的经销协议。2016年8月起,Orexigen公司开始在美国独立销售Contrave。2017年1月初,Orexigen公司启动了名为“减肥的幕后的大脑英雄”(Brains BehindWeight Loss)的消费者教育活动,以让消费者了解大脑在减肥中发挥的作用。该教育活动最终还是服务于Contrave的销售,因为Contrave就是作用于中枢神经系统。同样在1月初,Orexigen公司还公布了Contrave一项名为IGNITE研究的结果,进一步充实了Contrave的有效性与安全性依据。
虽然上市比Qsymia及Belviq晚,但Contrave潜在的市场规模似乎更加广阔,特别是EMA批准,使得Contrave成为欧洲市场除了奥利司他以外唯一的口服减肥药。Orexigen公司也在积极寻找经销合作方,布局Contrave的全球市场。单2016年,就与Valeant、Consilient HealthLtd、Biologix FZCO等公司签定了经销协议,涉及中欧与东欧18国以及土耳其、澳大利亚与新西兰、英国与爱尔兰、中东10国等多个地区的经销权。先前,韩国合作方Kwang Dong公司已经启动了Contrave在韩国的销售,并于2016年前9个月内贡献了290万美元的销售额。
Contrave在中国的核心专利见表12。
表12 Contrave在中国的核心专利
目前国内暂无企业申报Contrave,也无国外企业申报进口。
5. 利拉鲁肽注射液,商品名Saxenda-名门之后,表现不俗
Saxenda是由老牌糖尿病药物制药巨头诺和诺德公司推出的第一个注射用减肥药,该药的活性成分利拉鲁肽先前已于2010年1月获得FDA批准用于治疗Ⅱ型糖尿病(商品名Victoza),并已成为全球范围內销售最高的GLP-1类降糖药。借助于诺和诺德全球强大的销售团队以及Victoza已有的用药人群基础,Saxenda上市以来销售额迅速上升。根据诺和诺德2016年第3季度季报,2016年前三季度Saxenda的销售额约为14亿美元。当然,Saxenda每月近1000美元的用药成本,以及需要注射而给用药带来的不便,仍然会限制其在其他地区的市场拓展,特别是支付能力较低的地区。
Saxenda在中国的核心专利如表13所示。
表13 Saxenda在中国的核心专利
诺和诺德的利拉鲁肽注射液于2011年9月在中国上市,商品名诺和力(Victoza),用于降糖。
国内的深圳翰宇药业与杭州九源基因工程申报利拉鲁肽及其注射液,前者尚在审评,后者已获准临床。
三、总结
肥胖是一种慢性疾病,因此长期的体重控制对于改善公众健康水平减轻相关的经济负担至关重要。因此,药物治疗将在抗击肥胖及其相关的并发症中继续发挥着重要的作用。小编在本文中援引Dhiren K Patel等人的综述研究,以前相关的市场数据,对国内外常用的减肥药进行了综述。虽然肥胖症的发病形势日益严峻,但近几年上市的减肥新药的市场表现却不尽如人意,这与新药的价格过高、医疗保险未覆盖减肥药、医师的治疗重点等多种因素有關。各公司均针对目前的困局采取了一系列的措施,是否能行之有效,还有待时间的考验。
注:本文是投稿文章,文章内容仅代表作者本人观点,如有疑问可与作者邮件(williamxiang6107@sina.com)联系。转载本文请注明作者和来源,否则一律认定为侵权。


